Page 137 - 《广西植物》2024年第12期
P. 137
12 期 朱帮会等: 有齿鞘柄木根及茎的化学成分研究 2 2 9 5
H ̄7 / H ̄8 / H ̄9ꎬ结 合 HMBC 信 号 H ̄2、 H ̄6、 H ̄7 与
C ̄1 的相关信号ꎬH ̄7 与 C ̄1、C ̄8 的相关信号ꎬH ̄8
与 C ̄7、C ̄9 的相关信号ꎬ进一步确定化合物的平面
结构为 8ꎬ9 ̄dihydroxy ̄3ꎬ5ꎬ7 ̄trimethoxy phenicol ̄4 ̄
O ̄glucosideꎮ 化合物 1 通过进一步酸水解得到葡
萄糖ꎬ衍生化后进行 GC 分析ꎬ其保留时间( t =
R
29.05 min) 与 D ̄吡喃葡萄糖对照品一致ꎬ结合端
基质子的耦合常数 J = 8.4 Hzꎬ确定其苷键构型为
β 构型ꎬ确定该化合物中糖基为 β ̄D ̄吡喃葡萄糖ꎮ
经查阅文献ꎬ化合物 1 的 H ̄7 与 H ̄8 的相对构型
通过偶合常数 J = 5.4 Hz 及 C ̄7 与 C ̄8 的化学位移
之差为 8.7ꎬ 推测 H ̄7、H ̄8 的相对构型为赤式( 张
婷婷等ꎬ2015ꎻ闫建昆ꎬ2022)ꎮ 化合物 1 的实 验
CD 图谱和(7Sꎬ8S) 计算 ECD 图谱基本一致( 图
4)ꎬ从而确定其绝对构型为 7Sꎬ 8Sꎮ
1
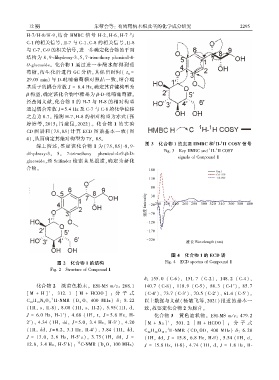
图 3 化合物 1 的主要 HMBC 和 H ̄ H COSY 信号
1
综上所述ꎬ鉴定该化合物 1 为(7Sꎬ8S) ̄8ꎬ9 ̄
1 1
Fig. 3 Key HMBC and H ̄ H COSY
dihydroxy ̄3ꎬ 5ꎬ 7 ̄trimethoxy phenicol ̄4 ̄O ̄β ̄D ̄
signals of Compound 1
glucosideꎬ经 Scifinder 检索未见报道ꎬ确定为新化
合物ꎮ
图 4 化合物 1 的 ECD 谱
图 2 化合物 1 的结构 Fig. 4 ECD spectra of Compound 1
Fig. 2 Structure of Compound 1
δ: 155. 0 ( C ̄6)ꎬ 151. 7 ( C ̄2)ꎬ 148. 2 ( C ̄4)ꎬ
化合物 2 淡黄色粉末ꎮ ESI ̄MS m / z: 268.1 140.7 ( C ̄8)ꎬ 118. 9 ( C ̄5)ꎬ 88. 3 ( C ̄1′)ꎬ 85. 7
[ M + H ] ꎬ 312. 1 [ M + HCOO ] ꎻ 分 子 式 ( C ̄4′)ꎬ 73.7 (C ̄3′)ꎬ 70.5 (C ̄2′)ꎬ 61.4 (C ̄5′)ꎮ
-
+
1
C H N Oꎮ H ̄NMR ( D Oꎬ 400 MHz) δ: 8. 22 以上数据与文献( 杨敏飞等ꎬ2021) 报道的基本一
10 13 5 2
(1Hꎬ sꎬ H ̄8)ꎬ 8.08 (1Hꎬ sꎬ H ̄2)ꎬ 5.95(1Hꎬ dꎬ 致ꎬ故鉴定化合物 2 为腺苷ꎮ
J = 6.0 Hzꎬ H ̄1′)ꎬ 4.68 (1Hꎬ tꎬ J = 5.6 Hzꎬ H ̄ 化合物 3 黄色油状物ꎮ ESI ̄MS m / z: 479.2
-
+
2′)ꎬ 4.34 (1Hꎬ ddꎬ J = 5.0ꎬ 3.4 Hzꎬ H ̄3′)ꎬ 4.20 [ M + Na ] ꎬ 501. 2 [ M + HCOO ] ꎻ 分 子 式
1
(1Hꎬ ddꎬ J = 6.2ꎬ 3.1 Hzꎬ H ̄4′)ꎬ 3.84 (1Hꎬ ddꎬ C H O ꎮ H ̄NMR ( CD ODꎬ 400 MHz) δ: 6. 28
22 32 10 3
J = 13. 0ꎬ 2. 6 Hzꎬ H ̄5′a)ꎬ 3. 75 ( 1Hꎬ ddꎬ J = (1Hꎬ ddꎬ J = 15.8ꎬ 6.8 Hzꎬ H ̄9)ꎬ 5.54 (1Hꎬ dꎬ
13
12.8ꎬ 3.4 Hzꎬ H ̄5′b)ꎻ C ̄NMR (D Oꎬ 100 MHz) J = 15.8 Hzꎬ H ̄8)ꎬ 4.74 (1Hꎬ dꎬ J = 1.8 Hzꎬ H ̄
2