Page 185 - 《广西植物》2023年第11期
P. 185
11 期 冯树慧等: 烟管头草的化学成分及其体外抗白血病活性研究 2 1 4 5
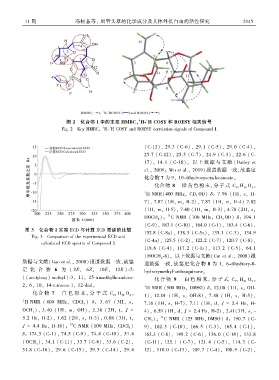
图 2 化合物 1 中的主要 HMBC、 H ̄ H COSY 和 ROESY 相关信号
1
1
Fig. 2 Key HMBCꎬ H ̄ H COSY and ROESY correlation signals of Compound 1
1
1
(C ̄13)ꎬ 29.3 ( C ̄6)ꎬ 29.1 ( C ̄5)ꎬ 29.0 ( C ̄4)ꎬ
25.7 (C ̄12)ꎬ 25.5 (C ̄7)ꎬ 24.9 (C ̄3)ꎬ 22.6 ( C ̄
17)ꎬ 14. 1 ( C ̄18)ꎮ 以 上 数 据 与 文 献 ( Dailey et
al.ꎬ 2009ꎻ Wu et al.ꎬ 2019)报道数据一致ꎬ故鉴定
化合物 7 为 9ꎬ 10 ̄dihydroxyoctadecanoateꎮ
化合 物 8 橙 黄 色 粉 末ꎬ 分 子 式 C H O ꎮ
15 10 5
1
H NMR(400 MHzꎬ CD OD) δ: 7.96 (1Hꎬ sꎬ H ̄
3
7)ꎬ 7.87 (1Hꎬ mꎬ H ̄2)ꎬ 7.87 (1Hꎬ mꎬ H ̄4) 7.82
(1Hꎬ mꎬ H ̄5)ꎬ 7.40 (1Hꎬ mꎬ H ̄3)ꎬ 4.78 (2Hꎬ sꎬ
13
HOCH )ꎻ C NMR (100 MHzꎬ CD OD) δ: 194.1
2 3
(C ̄9)ꎬ 183.1 (C ̄10)ꎬ 164.0 (C ̄1)ꎬ 163.4 (C ̄6)ꎬ
图 3 化合物 1 实验 ECD 与计算 ECD 图谱的比较
152.8 (C ̄8a)ꎬ 138.3 (C ̄5a)ꎬ 135.1 (C ̄3)ꎬ 134.9
Fig. 3 Comparison of the experimental ECD and
calculated ECD spectra of Compound 1 (C ̄4a)ꎬ 125.5 (C ̄2)ꎬ 122.2 (C ̄7)ꎬ 120.7 (C ̄8)ꎬ
118.6 ( C ̄4)ꎬ 117. 2 ( C ̄1a)ꎬ 113. 2 ( C ̄5)ꎬ 64. 1
(HOCH  ̄8)ꎮ 以上数据与文献(Cui et al.ꎬ 2008)报
数据与文献(Gao et al.ꎬ 2008)报道数据一致ꎬ故鉴 2
道数据一致ꎬ故鉴定化合物 8 为 1ꎬ 6 ̄dihydroxy ̄8 ̄
定 化 合 物 6 为 ( 2Eꎬ 6Zꎬ 10Eꎬ 12R ) ̄7 ̄
hydroxymethyl ̄anthraquinoneꎮ
[( acetyloxy) methyl] ̄3ꎬ 11ꎬ 15 ̄trimethylhexadeca ̄ 化 合 物 9 白 色 粉 末ꎬ 分 子 式 C H O ꎮ
15 10 5
2ꎬ 6ꎬ 10ꎬ 14 ̄tetraene ̄1ꎬ 12 ̄diolꎮ 1
H NMR (500 MHzꎬ DMSO) δ: 12.08 (1Hꎬ sꎬ OH ̄
化合 物 7 白 色 粉 末ꎬ 分 子 式 C H O ꎮ
19 38 4 1)ꎬ 12.01 (1Hꎬ sꎬ OH ̄8)ꎬ 7. 48 (1Hꎬ sꎬ H ̄5)ꎬ
1
H NMR ( 400 MHzꎬ CDCl ) δ: 3. 67 ( 3Hꎬ sꎬ
3 7.16 (1Hꎬ sꎬ H ̄7)ꎬ 7.11 (1Hꎬ dꎬ J = 2.4 Hzꎬ H ̄
OCH )ꎬ 3.40 (1Hꎬ mꎬ OH)ꎬ 2.30 (2Hꎬ tꎬ J = 4)ꎬ 6.59 (1Hꎬ dꎬ J = 2.4 Hzꎬ H ̄2)ꎬ 2.41(3Hꎬ sꎬ  ̄
3
5.2 Hzꎬ H ̄2)ꎬ 1.62 (2Hꎬ sꎬ H ̄3)ꎬ 0.88 (3Hꎬ tꎬ CH )ꎻ 13 C NMR (125 MHzꎬDMSO) δ: 190. 7 ( C ̄
3
13
J = 4.4 Hzꎬ H ̄18)ꎻ C NMR (100 MHzꎬ CDCl ) 9)ꎬ 182. 3 ( C ̄10)ꎬ 166. 5 ( C ̄3)ꎬ 165. 4 ( C ̄1)ꎬ
3
δ: 174.3 (C ̄1)ꎬ 74.5 (C ̄9)ꎬ 74.4 ( C ̄10)ꎬ 51.4 162.3 (C ̄8)ꎬ 149.2 ( C ̄6)ꎬ 136.0 ( C ̄14)ꎬ 133.8
( OCH )ꎬ 34.1 (C ̄11)ꎬ 33.7 (C ̄8)ꎬ 33.6 (C ̄2)ꎬ (C ̄11)ꎬ 125. 1 ( C ̄7)ꎬ 121. 4 ( C ̄5)ꎬ 114. 3 ( C ̄
3
31.8 ( C ̄16)ꎬ 29. 6 ( C ̄15)ꎬ 29. 5 ( C ̄14)ꎬ 29. 4 12)ꎬ 110.0 ( C ̄13)ꎬ 109.7 ( C ̄4)ꎬ 108.9 ( C ̄2)ꎬ